>Top Periodic Table (周期律表) |
+Ia+ |
IIa |
IIIb |
IVb |
Vb |
VIb |
VIIb |
VIII |
Ia |
IIa |
IIIa |
IVa |
Va |
VIa |
VIIa |
O |
H |
+++ |
+++ |
+++ |
+++ |
+++ |
+++ |
+++ |
+++ |
+++ |
+++ |
+++ |
+++ |
+++ |
+++ |
+++ |
+++ |
He |
Li |
Be |
|
|
|
|
|
|
|
|
|
|
B |
C |
N |
O |
F |
Ne |
Na |
Mg |
|
|
|
|
|
|
|
|
|
|
Al |
Si |
P |
S |
Cl |
Ar |
K |
Ca |
Sc |
|
V |
Cr |
Mn |
Fe |
Co |
Ni |
Cu |
Zn |
Ga |
Ge |
As |
Se |
Br |
Kr |
Rb |
Sr |
Y |
Zr |
Nb |
Mo |
Tc |
Ru |
Rh |
Pd |
Ag |
Cd |
In |
Sn |
Sb |
Te |
I |
Xe |
Cs |
Ba |
La* |
Hf |
Ta |
W |
Re |
Os |
Ir |
Pt |
Au |
Hg |
Tl |
Pb |
Bi |
Po |
At |
Rn |
Fr |
Ra |
Ac** |
+↑Isthmus
(d-block) +++++++++++++ ↑Eastern rectangle (p-block) |
↑Western
Rectangle (s-block)+++++↓Southern
Island (f-block) |
Lanthanoid * |
La |
Ce |
Pr |
Nd |
Pm |
Sm |
Eu |
Gd |
Tb |
Dy |
Ho |
Er |
Tm |
Yb |
Lu |
|
Actinoid ** |
Ac |
Th |
Pa |
U |
Np |
Pu |
Am |
Cm |
Bk |
Cf |
Es |
Fm |
Md |
No |
Lr |
|
|
>Top 1. The Terrain:
- The Periodic Kingdom:
This is a land of the imagination. This is the kingdom of the chemical
elements. It is not an extensive country, for it consists of only
a hundred or so regions, yet it accounts for everything material
in our actual world.
- The kingdom is not an amorphous jumble of regions, but a closely
organized state in which the character of one region is close
to that of its neighbor.
- The landscape is largely characterized by transitions; savannah
blends into gentle valleys, which gradually deepen into almost
fathomless gorges; hills gradually rise form plains to become
towering mountains.
- From overhead we see that it stretches in a great vista, from hydrogen to beyond distant uranium. There are the
glittering, lustrous regions made up of metals and lying together
in the Western Desert. How remarkable it is that these desert
lands make up so much of the kingdom supplies such luxuriance
in the real world!
- The Eastern landscape:
To the east, the landscape varies markedly. The lake is not the
limpid gray or blue of Earthly lakes, but a striking deep red, verging
on brown. This region is known as bromine.
The other lake is quite different in appearance, with a harshly
metallic, silvery sheen. This is mercury,
a liquid lake amidst the stone.
|
1.元素の土地:
- 周期律の王国:
ここは想像上の土地である。化学元素の王国なのだ。ここはそれほど広い国ではない、というのも百余の地域からなるに過ぎないからである。だが我々の現実の世界のすべての物質について説明できるのである。
- この王国はまとまりのない混乱した地域ではない。それは緊密に組織化され、ある地域の特徴は隣接地域のそれと近似しているのである。
- 地形は全体として移り変わる所に特徴がある。サバンナは徐々に渓谷に移り変わり、丘は段々と平原を形成し、やがては聳える山脈になる。
- 上空から見ると水素からウランに至るまで広大な展望が広がっているのが見える。西側の砂漠地帯には金属からなるきらきらと光沢のある地域が横たわっている。王国の大半を占めるこれら砂漠地帯が現実世界の豊かさを支えていることは注目に値する。
- 東部地域:
東部の方面は、地形は際だった変化に富む。湖は地球の湖のように透明の灰色や青色ではなく、目立つ深い赤色で縁は茶色である。この地域は臭素として知られている。もう一つの湖に見かけは全く異なり、荒々しい金属色に見える銀色の輝きである。それは水銀であり、岩石の真ん中にある液体の湖である。
|
>Top The Western desert:
- has gradually modulated into regions that are seemingly metallic
but have a softened personality. Such elements include silicon and arsenic. and less familiar
regions of the kingdom such as polonium and tellurium.
- There is the familiar vivid splash of sulfurous yellow. Its neighbor selenium varies, from metallic
gray in one form to ruby red in another. Carbon also has remarkable variety; its most familiar form is sooty
black, but it can modulate to sparkling diamond, gray metallic
graphite, and the orange-brown of a recently discovered crystalline
fulleite (C60, 1985).
- The colors of the landscape become even more varied near the
eastern coastline. Most striking of all are the halogens; south
of red lake of bromine lies the lustrous purplish-black iodine.
And south of iodine lies astatine.
This part of the kingdom attracts the eye with its pleasing
hues.
|
西部の砂漠:
- そこは徐々に金属的に見える地域から柔らかな性質を持つ地域へと変化している。これらの元素の中には珪素や砒素が含まれ、またあまり有名でないポロニウムやテルルのような地域となる。
- よく知られた派手な硫黄の黄色がある。その隣のセレンはある時はメタリックな灰色からルビーの赤色へと変化する。炭素もまた顕著な変化をする。通常はすすけた黒色であるが、
輝くダイヤモンドへと変化したり、メタリックな灰色のグラファイトや最近発見された橙・茶色の結晶のフラーレン (fulleite)
がある。(C60, 1985発見)
- 東部海岸線近くに行くにつれて地形の色は一層変化してくる。もっとも印象的なのはハロゲンである。臭素の赤い湖の南には光沢のある紫・黒色のヨウ素あり、その南側にはアスタチンがある。王国のこの部分の色相は目を見張るものがある。
|
 |
>Top The Northeastern landscapes:
- seem less fertile in appearance than the Western Desert. But the
northeastern coast is far from useless, for here lies oxygen.
Oxygen is the essence of animation. Its western neighbor, nitrogen,
is also apparently essential to life. Nitrogen fixation had to be
achieved long before, because proteins are built from it.
- The regions of the eastern coast are a different matter (once
called the rare gases); they are largely inactive. Argon is more abundant in more abundant in the Earth's atmosphere than
carbon dioxide. Helium,
while rare in our atmosphere, is far from rae in the universe,
where it makes up 25% of all. And radon,
far south, is dangerously abundant in parts of the Earth where
natural radioactivity occurs.
- Note: Radon
is used as an indication of exploration of radioactive minerals.
- North of the mainland lies a single, isolated region - hydrogen.
This simple but gifted element is an essential outpost of the
kingdom, for despite its simplicity it is rich in chemical personality.
It is also the most abundant element in the universe.
|
北東部の地形:
- そこは見かけ上は西部砂漠地帯より不毛に見える。しかし北東海岸には非常に有用な元素がある。そこには酸素がある。酸素は活気の源である。その西隣は窒素があり、これもまた明らかに生命にとって必須の元素である。窒素の固定はかなり以前から行われてきた。それはタンパク質がその窒素固定で作られるからである。
- 東部海岸の地域は異なる物質からなる。 (かつては希ガスと呼ばれた)それらは概して不活性である。アルゴンは地球の大気中の二酸化炭素よりも多い。ヘリウムは、大気中にはまれだが、宇宙には豊富にあり、全元素の25%を占める。南端にあるラドンは、地球上では天然の放射能の高い一部の地域では危険なほど豊富にある。
- 注)ラドンは放射性鉱物の探鉱の指標として利用される。
- 主大陸の北側には、水素が孤立して存在する地域がある。単純だが優れた元素はこの王国の先端の地にある。またその単純性にもかかわらず化学的性質は豊富であり、宇宙では最も豊富にある元素でもある。
|
>Top 2. Products of the regions:
- The Isthmus: (Transition element)
Sc |
|
V |
Cr |
Mn |
Fe |
Co |
Ni |
Cu |
Y |
Zr |
Nb |
Mo |
Tc |
Ru |
Rh |
Pd |
Ag |
La* |
Hf |
Ta |
W |
Re |
Os |
Ir |
Pt |
Au |
Invisibility does not mean uselessness. Likewise, the regions of
the almost uniform metallic desert are rich sources of fecundity.
- For instance, one region of the Western Desert is iron,
the element that helped to lift humanity out of the Stone Age
and impel it toward and through the Industrial Revolution. By
forming alliance with a number of its neighbors, such as cobalt, nickel, vanadium,
and manganese, iron became
steel. The fact that iron is able to form alliances so readily
with its neighbors is a point not to go unnoticed.
- A few steps to the east of iron lies copper,
which - because it could be extracted so easily from its ores -
was the first element to be used on our long journey out of the
Stone Age. Copper is moderately resistant to the unwanted chemical
change we term corrosion; in water pipes, and in alliance with the
nearby regions of bronze and nickel in coinage.
- Close to copper lie silver and gold, which have long
been used as metals of commerce, decoration, and coinage, partly
because of their attractive appearance and their rarity but also
because they, too, are resistant to corrosion.
- The Western Desert was explored and exploited from east to
west; Copper displaced stone to give us the Bronze Age. Then
they encountered the region of iron and used it to fabricate more
effective weaponry.
- Deep in the Western Desert, they finally stumbles upon titanium,
a remarkable prize indeed. This is a metal that is tough and resistant
to corrosion, yet light. Titan, and its neighbors vanadium and molybdenum, in alliance
with iron, form the durable steels.
- The Isthmus, which links two rectangular blocks at the kingdom's
western and eastern extremes, has provided so many of the workhorses
of our society.
|
2. 各地の生産物:
- 地峡ブロック (遷移元素):
見えないことが無用を意味するものではない。同様に、ほとんど一様に見える金属の砂漠も豊かな資源に富む土地なのである。
- 例えば、西部砂漠に鉄の地域がああり、この元素は人類を石器時代から引き上げ、更に産業革命にまで駆り立ててくれた。その多くの隣接する元素であるコバルト、ニッケル、バナジウム、マンガンなどと連合することで鉄は鋼鉄となった。鉄がその隣人をこれほど連合することができるということはもっと注目されて良い。
- 鉄の地域より少し東側には銅がある。銅は鉱石からの抽出がが容易にできたので石器時代から我々が抜け出す長い旅路でまず最初に利用した元素であった。銅は我々は腐食と呼ぶ好ましくない化学変化にある程度抵抗できるので、水道管として、また近くの地域の元素と合金を作って青銅や白銅としてコインで使用されている。
- 銅の近くには銀と金があり、これらは長く取引や装飾、貨幣として利用されてきた。それは魅力的な外見や希少であるのが理由の一部ではあるが、腐食に強いということもその理由である。
- 西部地域は東から西へ向かって探鉱開発が進んでいった。銅は石に代わって我々に青銅器時代をもたらした。その後我々は鉄と遭遇し、さらに効果的な武器製造に利用するようになった。
- 西部砂漠の奥地で、我々は偶然チタンに出会う。それは実にすばらしい贈り物であった。これは丈夫で腐食に強く、しかも軽量であった。チタンおよび隣接するバナジウムやモリブデンは鉄を合金を作ると丈夫な鋼鉄が得られる。
- 王国の東西2つのブロックを連結する地峡は、我々の社会に大いに利用されてきた。
|
>Top Alkali metals:
-
Li |
Be |
Na |
Mg |
K |
Ca |
Rb |
Sr |
Cs |
Ba |
Fr |
Ra |
The Western Rectangle are the metals that are never found native
(free form) in nature, because they are highly reactive. Most of
these metals are too virulent even to touch. What happens when it
rains in their regions.
- In the region of lithium,
rain has little effect. Certainly the terrain simmers and bubbles
with hydrogen gas.
- This is not so with sodium.
Here rain and terrain are in violent conflict; the ground seethes
and boils whenever a raindrop strikes. If rain is tolerable
in the region of lithium and scarcely bearable of sodium, rain
in potassium is beyond
belief. It ignites and burns.
- And still further south? Now rain is explosive. In the regions
of rubidium and cesium,
each raindrop is a bomb. The trend in this family of elements
is of increasing chemical reactivity from north to south.
- Sodium and potassium are essential components of the activity
of the nervous system and brain.
- Alkaline earth metals:
Just to the east of the alkali metals lies another group of regions
with closely related properties. Calcium,
which also seethes when it rains, quietly bubbling and forming hydrogen
rather as lithium does. Calcium is a component of nervous activity,
like sodium and potassium. It is a component of such materials as
the bone (calcium phosphate) of endoskeletons and the shells (calcium
carbonate) of exoskeletons.
- Humans have quarried limestone and constructed buildings that
have lasted thousands of years.
- Magnesium is less reactive
than calcium; when it rains here, the terrain remains largely
unchanged. But magnesium can act. A particularly important product
of magnesium is an organic molecule called chlorophyll, which
contains a single magnesium atom at its eye. Chlorophyll holds
its magnesium eye to the sun and capture the energy of sunlight,
in the first step of photosynthesis.
- At the southern end of this family are the metals strontium, barium, and radium.
Radium is highly radioactive, and is used to kill unwanted proliferating
cells. A radioactive form of strontium-90 is a component of nuclear
fallout, and if it accumulates in place of calcium in bone it
can kill cells and induce leukemia.
|
アルカリ金属:
- 西部長方形ブロックは、天然にはそのままでは存在しない金属から成る。というのはそれらは活性度が高いからである。これらの多くは毒性が強く触ることができない。この地域に雨が降るとどうなるか。リチウムの地域では、雨の影響はそれほどでもない。確かに土地はシュウシュウと煮えて水素ガスを発生する。
- ナトリウムだとはそうはいかない。雨と土地とは激しく反応する。雨粒が降っている間中、土地は泡立ち沸騰する。雨にリチウムの地域であれはまだそれほどでもないが、ナトリウム地域ではほとんど耐えられないほどであり、カリウム地域となるともっと極端になる。そこでは発火して燃焼する。
- さらに南部へ行くとどうなるか。もはや雨は爆発を起こす。ルビジウムやセシウムの地域では、雨粒の各一粒が爆弾となる。この族の元素の化学反応の傾向は北から南へ行くほど激しくなる。
- ナトリウムとカリウムは神経系および大脳の活動にとって必須の元素である。
- アルカリ土類金属:
アルカリ金属の直ぐ東隣には、よく似た性質を持つ族が存在している。カルシウムもまた雨に対して反応し、静かに泡をだしてリチウムと同じように水素ガスを放出する。カルシウムはナトリウムやカリウムと同様に神経系の構成要素である。またそれは内骨格生物の骨の要素となり
(リン酸カルシウム) 、また外骨格生物の殻となる (炭酸カルシウム)
- 人類は石灰岩を採石して何千年も残る建築物を建設してきた。
- マグネシウムはカルシウムほどは反応しない。そこに雨が降ってもその土地は大きくは変わらない。しかしマグネシウムは反応できる。マグネシウムの特に重要な生成物は葉緑素と呼ばれる有機化合物であり、その中心部の目
(*ホルフィリン環) の所にマグネシウム原子がある。葉緑素はマグネシウムの目を太陽にかざして、光合成の最初の段階として太陽光のエネルギーを吸収する。
- この属の南端には、ストロンチウム、バリウム、ラジウムの金属がある。ラジウムは高い放射性を示し、不要な増殖細胞を殺すのに利用される。放射性物質であるストロンチウム-90は核爆発の降下物であり、もしそれが骨中のカルシウムを置換して蓄積すると細胞を破壊して白血病を引き起こす。
|
>Top Silicon:
- Immediately to the south of carbon lies silicon.
Like carbon, but to a lesser degree, silicon is capable of forming
some of the long-chain molecules needled in any process as complex
as life. The recent alliance of the two regions, in which carbon-based
organisms have developed the use of silicon-based artifacts for
information technology. One day silicon may well overturn the suzerainty
of its northern neighbor and assume the dominant role. It certainly
has long-term potential, for its metabolism and replication need
not be as messy as carbon's.
- Whereas the metals of the western coastline are so vigorous, here
on the desert's eastern annex the metals are much calmer; chemically
indifference. Tin, for example, was
once applied as a protective coating to steel cans, before aluminum
displace both skeleton and skin for the almost universal packaging.
- Isthmus: (Transition element)
The distinction between the metal of the eastern and western fringes
suggests that the Isthmus forms a transitional bridge between the
two. Scandium in the west
is a violet metal, whereas copper is calm. There are certain technical
reasons that exclude zinc, cadmium, and mercury for this appellation.
-
B |
C |
N |
O |
F |
Ne |
Al |
Si |
P |
S |
Cl |
Ar |
Ga |
Ge |
As |
Se |
Br |
Kr |
In |
Sn |
Sb |
Te |
I |
Xe |
Tl |
Pb |
Bi |
Po |
At |
Rn |
At the diagonal border of the Western Desert - there is an ambiguous
zone of elements known as metalloids, which possess metallic and
nonmetallic characteristics. It is probably no coincidence that
this ambiguous territory includes the elements that make possible
the most complex properties of all, life and consciousness.
|
ケイ素:
- 炭素の南隣にはケイ素がある。炭素に似て、程度はさほどでないが、ケイ素も生命の場合と同様に複雑なプロセスに必要な長い分子鎖を作ることができる。この2つの領域は最近連合が進んでいる。それは炭素を基礎にした有機物が情報技術をケイ素を基盤とする人工物の利用を発展させたからである。いつの日かケイ素が北の隣人の権力を逆転させ支配権を得るかもしれない。その理由としてはケイ素の代謝と複製は炭素の場合のように面倒なことが必要ないからである。
- 西海岸の金属はすべて活性化しているのに対し、砂漠の東側に付属地帯の金属はより不活性である。例えば錫は以前は鋼鉄製の缶詰の保護コーティングに利用されていたが、やがてアルミニウムが、ほとんどすべての缶詰の骨
(鋼鉄) も皮 (錫) も置き換わってしまった。
- 陸峡(遷移元素):
東部と西部の両端にある金属の際だった差は、その間にあるのが2つをつなぐ転移的な陸橋である。西側のスカンジウムは激しい金属だが、一方は銅は穏やかである。この名称の中に亜鉛、カドミウム、水銀が除かれているのは、ある種の技術的な理由がある。
- 西部砂漠の対角線上の境には、金属と非金属の性質を併せ持つ半金属として知られる曖昧な地域が存在する。この曖昧な地域の中には生命や意識に関する最も複雑な特性を可能にする元素が含まれている。
|
>Top 3. Physical Geography:
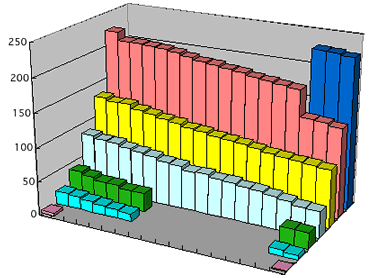 Atom's mass: Atom's mass:
Atom's mass lie between about 1 x 10^-31 and 1 x 10^-29 Kg. Modern
chemists termed atomic weights (atm): carbon is 12, then hydrogen
is 1, uranium is 238, and so on.
- The terrain of the kingdom in terms of altitudes that represent
the relative masses of the atoms, as sloping up from the northwest
tip to the dangerously radioactive regions of the far southeast.
The Southern Island slopes up from west to east, too, and the
southernmost strip of the island is uniformly higher than its
northern strip. There are a few places where this trend in altitude
will trip a careless walker, between tellurium (127.60) to iodine
(126.90), and between cobalt (59.93) and nickel (58.69); here
the land falls away very slightly instead of rising.
|
3. 物理的特徴の地形:
- 原子質量:
原子の質量はおよそ、 1x10^-31から 1x10^-29 Kg の間にある。近代化学は原子質量単位(amu)を定義した。炭素を12とすると、水素は1,ウランは238という具合にである。
- この王国の原子質量を高さで表示すると北西の端から放射性元素のある南東の端まで徐々に上昇していく。南の島は西から東へと下降する。南側は北側に比べ一様に高くなっている。山歩きする者にとって注意しなければならない場所がいくつかある。テルル (127.60) とヨウ素 (126.90) の間とコバルト (59.93) とニッケル (58.69) の間である。ほんの少しではあるが、この間は上昇ではなく下降している。
|
>Top Atom's diameter:
- The diameter of a typical atom is about 0.3nm. So the landscape
draped in altitude denoting diameter is much flatter than the landscape
of atomi
 c masses. The diameters are based on the lengths of the
bonds the elements form. Broadly speaking, the landscape of diameters
rises from north to south and falls from west to east, but there
are many exceptions. c masses. The diameters are based on the lengths of the
bonds the elements form. Broadly speaking, the landscape of diameters
rises from north to south and falls from west to east, but there
are many exceptions.
-
Note: Effective diameter of
metallic elements is a distance between adjoining atoms, and
that of nonmetallic elements is a distance between covalent
bond. Unit is in angstrom. (Source: Rikanenpyo, Chronological
Table of Science, 2001)
- Atom's density:
The altitude of this imaginary sheet sweeps upward from the Northwestern
Cape at lithium toward lead on the south east fringe of the desert.
The rise is not uniform, and a particular feature is the the high
mountain ridge which peaks at osmium (22.57) and iridium (22.42)
. In contrast, the density of magnesium is only 3 g/cm3.
|
原子半径:
- 典型的な原子の半径は0.3nm である。原子半径を基に地形を高さで表示すると、原子質量の場合よりも遙かに平坦になる。直径は原子結合の長さに基づく。大まかに言えば、原子半径に基づく地形は北から南へ向かって上昇し、西から東へ向かって下降しているが、例外も多い。
- 注)金属の場合の有効半径は隣接する原子間の距離、非金属の場合は共有結合の原子間隔。値のない場合は0とした。単位はA°
(理科年表2001による)
- 原子密度:
この原子密度に基づく地形の高さはリチウムのある北西端から鉛のある砂漠の南東の端に向けて上昇する。上昇は一様ではないが、特徴としてはオスミウム
(22.57) イリジウム (22.42) の所が山頂になっていることである。反面、マグネシウムの密度は3 g/cm3 に過ぎない。
|
>Top Atom's ionization
energy:
-
Positively charged ions are known as cations, while negatively
charged ones are as anions. Ion is the Greek word for
"travailing"; "cat" is derived from
the Greek for "down" and "an" from
the Greek for "up". The landscape will show the ease
with which atoms form ions . As so much of chemistry involves
the formation of ions, this landscape is very close to the depiction
of actual chemical properties. As we shall see, there are complex
and subtle rhythms of the land, yet they are explicable rhythms,
not random variations.
-
We shall consider only the first ionization
energy, the energy required to remove the first electron from
a neutral atom. The energy required to remove a second electron
is always higher than that the first electron from an electrically
neutral atom.
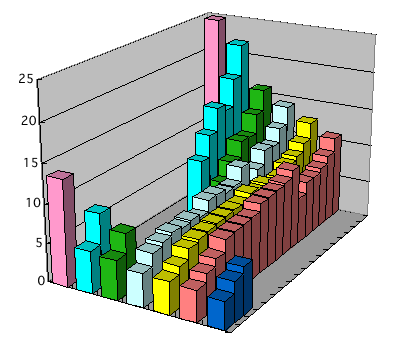
The broad trend is the ionization energy
generally increase from west to east across the kingdom and
decrease from north to south. The ionization energy of hydrogen
is 13.6 eV. The three highest peaks in the distance are helium
(24.6), neon (21.6), and fluorine (17.4). The low terrain
of the Western Desert should not come as a surprise; they
conduct an electric current, that is, the atoms that lie packed
together in the solid release electrons to a common pool that
lies like an ocean among the resulting cations.
|
原子のイオン化エネルギー:
- プラスに帯電してイオンは陽イオンと言い、マイナスに帯電したのは陰イオンである。イオンとはギリシャ語で「旅するもの」の意であり、陽イオンのcationの"cat"とは下という意味であり、また陰イオンのanionの"an"とは上という意味である。この地形は原子がイオンになりやすさに基づいている。化学では多くはイオンを形成しているので、この地形は実際の化学的特性の描写に非常に近い。この地形で見るように複雑ではあるがランダムではない、まだうまくは説明できない点もあるが地形の微妙なリズムが見られる。
- ここでは第一イオン化エネルギー、すなわち中性の原子から最初の電子を取り出すのに必要なエネルギーだけに注目する。二番目の電子を取り出すエネルギーは中性の原子から取り出す最初の電子の場合より常に大きい。
- イオン化エネルギーの大まかな傾向としては、王国の西から東に向かって増加し、北から南へ向かっては現象する。水素のイオン化エネルギーは13.6
eV である。遠方に見える3つの頂上はヘリウム (24.6)、ネオン (21.6)、およびフッ素 (17.4) である。西部の低地は驚くべきことではない。それらは電導体、即ち固体として原子が密集しており電子は共通にプールされていてあたかも陽イオンの間の大洋のようになっているのである。
|
>Top 4. History of discovery:
- The history of discovery:
The discovery of many elements is lost in antiquity. Which genius
first isolated copper and opened the way to the progress of civilizations?
Who first identified iron? No one knows. The names of the Drakes,
the Magellans, the Cabots, and the Cooks of chemistry come down
to us only from 17C.
- The discovery of new elements has depended on the development
of new technologies, and these newly discovered elements have in
turn given rise to even newer technologies.
- The first enabling technology was fire. Fire itself, when carefully
controlled and no more vigorous than resulting in a gentle charring,
led to the isolation of carbon as charcoal,
which in turn could be used in combination with fiercer fires to
react with other stones, thereby freeing new material.Tin, lead and other regions of
the Isthmus were discovered in this way.
- A few elements - most evidently gold, copper, and sulfur - can be found in native form.
- Hydrogen is found hardly
at all in its native state on earth, except for pockets of pure
hydrogen gas trapped below ground by rock formations. The cosmic
ubiquity of hydrogen was not recognized until early 20C.
- Oxygen was discovered in
1774. Joseph Priestley, 18C English chemist used a lens to focus
the heat of the sun onto a phial of mercury oxide and generate bubble
of a life-giving gas. The Swedish chemist Karl Scheele in fact discovered
oxygen two years before Priestley, but delays in publication lost
him the priority he deserved.
-
At the beginning of 19C came a very special technological advance.
Electrolysis is the breaking down of matter by the passage of an
electric current through it. Humphry Davy applied an electric current
to molten caustic potash (potassium hydroxide), and obtained beads
of a silvery reactive metal that he named potassium.
Davy had the wit to apply the same technique to a similar compound,
caustic soda (sodium hydroxide), and obtained the northern neighbor
of potassium, which he named sodium.
- Magnesium was culled in
1808, calcium and strontium also in 1808 by Davy.
- Explorers mapped the eastern promontory of the halogens, bring back
knowledge of chorine discovery
by Scheele in 1774 and bromine by Antoine-Jerome Balard in 1826. Fluorine,
the peak of the mountain range of reactivity was added by Henri
Moissan in 1886.
|
4.発見の歴史:
- 発見の歴史:
多くの元素が古代からどう発見されたのかはわからない。どの天才が最初に銅を取り出して文明への道を切り開いたのだろうか。誰が最初に鉄を発見したのだろうか。ドレーク、マゼラン、カボット、クック達に匹敵するのような発見者の名前は17世紀以降になってからである。
- 新たな元素の発見は新たな技術の発展に依存してきた。そしてこれら新元素の発見が今度はさらに新技術を発展させてきたのである。
- 最初の利用技術は火であった。火自身は、注意深く制御して活発な燃焼をさせないで炭化することで木炭のように炭素を分離できる。今度はこの木炭を利用して他の石にさらなる火力を組み合わせることで新物質である錫、鉛など陸橋の他の地域の元素を発見することができた。
- 金、銅、硫黄などいくつかの元素はそのまま天然に産出する。
- 水素は地球上ではほとんどそのままでは見いだせない。例外的には造岩作用によって地中に純粋な水素ガスが捕集されている場所がある。宇宙には水素は普遍的に存在していることは20世紀初頭まで認識されなかった。
- 酸素は1774年に発見された。英国の科学者であるJ.プリーストリーは太陽光をレンズで集光し、酸化水銀の瓶に照射することで生命のガスの泡を発生させた。スウェーデンの科学者カール・シューレは実際にはプリーストリーより2年早く発見していたが、発表が遅れたため優先権を受けられなかった。
- 19世紀の初頭には、特殊な技術的進歩があった。電気分解は電流を流すことによって物質を分解する方法である。ハンフリー・デイビー
(英) は融解した苛性カリ (水酸化カリウム) に電流を通して 、ビーズ状の銀色の反応の早い金属を得た。彼はこれをカリウムと命名した。デイビーは同じ技術を同様の物質である苛性ソーダ
(水酸化ナトリウム) にも応用してカリウムの北隣のナトリウムを得た。
- 1808年にマグネシウム、また同年にカルシウムおよびストロンチウムがいずれもデイビーによって抽出された。
- 東側の岬であるハロゲン元素の探査が行われ1774 年にはシェーレ (スウェーデン) によって塩素の発見がもたらされた1826年にはA.J.バラール
(仏) は臭素を、そして反応元素の山脈の頂点であるフッ素は1886年にアンリ・モアッサン
(仏)が発見した 。
|
>Top Dmitri Mendeleev:
- The Russian chemist Dmitri Mendeleev, who is one of the principal
historical figures of the kingdom and who in 1869 essentially laid
it out in its current form, showed the power of this approach to
discovery. He recognized a gap close to silicon, which, for want
of a name, he called eka-silicon (eka being the
sanskrit name for the numeral 1) When germanium was discovered by Clemens Winkler in 1886, it was found that Mendeleev
had been substantially correct. The same was true for eka-boron
(scandium not isolated until
1936) and eka-aluminum (gallium,
isolated in 1875).
- Marie Curie in collaboration with her husband, Pierre, isolated radium from tons of pitchblende,
a uranium ore, based on her knowledge of barium, its northern neighbor.
- The western peaks of activity were mirrored on the eastern fringe
of the Eastern
Rectangle. But this symmetry of the kingdom was an
illusion, because at the base of the halogen cliffs lay the littoral
of the rare, later inert, and now noble gases. Argon (Greek word for 'lazy') is far from rare, being even more abundant
in the atmosphere than carbon dioxide. The discovery of argon led
to the realization that there were more regions in the area, and neon, krypton,
and xenon were soon
discovered, all
of them by William Ramsay in 1898. Helium makes up about 25% of the universe, yet it lurked invisible and
unnoticed until 1868, when it was observed spectroscopically during
a solar eclipse. Liquid helium is essential to cryogenics and cryotechnology,
and until recently it was the only route to the achievement of superconductivity.
Once again it was William Ramsay isolated the radioactive gas radon in 1908.
- At the start of the Manhattan Project of 1940s, the aim of which
was to construct an atomic bomb, the Southern Island terminated
at uranium. Uranium had the
potential to beget new elements when appropriately organized in
what are now called nuclear reactors; uranium begat neptunium and plutonium. More recently
still, reclamation has proceeded by synthesis.
+U |
Np |
Pu |
Am |
Cm |
Bk |
Cf |
Es |
Fm |
Md |
No |
Lr |
- The highly transient elements of the mainland's southern shore
have been made in machines of cyclotrons, synchrotrons, and linear
accelerator (LINAC): 104 rutherfordium,
105 dubnium, 106 seaborgium 107 bohrium,108 hassium,
109 meitnerium, and 110 darmstadtium,
(then 111 unununium, 112 ununbium,
113 ununtrium, 114 ununquadrium,
115 ununpentium, 116 ununhexium,
117 ununseptium, 118 ununoctium).
- Note: The above latest elements described
in the book are updated.
|
D. メンデレーエフ:
- ロシアの化学者であるD.メンデレーエフは、この王国の歴史的に主要な概念を表し、1869年に現在の形式を提唱し、その後の発見の有力な道筋を示した。彼はケイ素に近い所の未知の元素を認識してエカ・シリコンと呼んだ。(
'eka' とはサンスクリット語で1番という意味) 1886年にC. ウィンクラーがゲルマニウムを発見したが、それはメンデレーエフが正しかったことを示した。またエカ・ボロン
(=スカンディウム、1936年分離)や、エカ・アルミニウム (=ガリウム、1875年分離)も同様であった。
- マリー・キューリーは夫のピエールと共同でウラン鉱石であるピッチブレンドからラジウムを分離したのも、その北隣のバリウムの知識に基づいている。
- 活性の西側の山頂は東部四角形の東端の峰と鏡面対称になっている。しかし王国のこの対称形は幻想であった。ハロゲンの崖の下には希ガス、不活性ガス、後には貴ガスと呼ばれるガスの沿岸地域を作っていたのである。アルゴン (ギリシャ語で'lazy' の意) は希れというにはほど遠く、大気中には二酸化炭素より多く存在する。アルゴンの発見はその地域にさらにネオン、クリプトン、キセノンの発見につながる。これらはすべてW.ラムゼー
(英) によって1898 年に発見された。ヘリウムは宇宙の25%を占めるが、なかなか見つからずようやく1868年の太陽日食のときの分光器分析で発見された。液体ヘリウムは低温処理や低温技術にとって必須であり、今まで超伝導への到達の唯一の道であった。W.
ラムゼーは1908年に再び放射性ガスであるラドンを分離した。
- 1940年代の原爆製造を目的としたマンハッタン・プロジェクトの開始時点では、南島はウランで終わっていた。ウランは、現在原子炉と呼ばれる中でうまく組織化されると新たな元素を生じる。ウランからネプツリウムやプルトニウムが生成される。さらにその後も合成によって開発が進んだ。
- 本土の南岸の短命の元素がサイクロトロン、シンクロトロン、線形加速装置 (LINAC)などと装置で生成されてきた。104番元素ラザフォーディウム、105番ドブニウム、106番シーボーギウム、107番ボーリウム、108番ハッシウム、109番マイトネリウム、110番ダルムシュタティウム、さらに111番ウヌヌニウム、112番ウヌンビウム、113番ウヌントリウム、114番ウヌンクアドリウム、115番ウヌンペンティウム、116番ウヌンヘキシウム、117番ウヌンセプティウム、118番ウヌンオクティウム
|
103
Lr |
|
105
Db |
106
Sg |
107
Bh |
108
Hs |
109
Mt |
110
Ds |
111
Uuu |
112
Uub |
113
Uut |
114
Uuq |
115
Uup |
116
Uuh |
117
Uus |
118
Uuo |
|
>Top 5. Naming of the elements:
- Once exploration of the kingdom became a science, the nomenclature
of the regions became systematized to a certain extent.
- The ancient names, whose origins are lost or only faintly discernible
in the mists of history.
- Sulfur S: from the Sanskrit sulvere
- Iron Fe, Gold
Au , & Silver Ag: from
Anglo-Saxon iron, gold, and seolfor.
- Copper Cu: from Latin cuprum,
from Cyprus, where much was found.
- Sodium Na & Potassium
K : Humphry Davy named after their respective source, soda and potash.
- Calcium Ca: calcium is present
in lime; from Latin calx.
- Magnesium Mg: from a white earth, magnes carneus, found in Magnesia, a district in ancient
Thessaly.
- Nitrogen N: from Greek nitron plus genos, or "niter giver" is named in recognition
of its occurrence in nitrates.
- Oxygen O: from Greek oxys,
acidic; Oxygen was widely believed to be a universal constituent
of acids. That view has since been overthrown, but the names of
elements stick. (Cf: hydrochloric acid)
- Some elements have been named on the basis of their color.
- Chlorine Cl: a pale yellow-green
gas, from Greek chloros (yellowish-green)
- Iodine I: a violet solid, from
Greek ioeides (violet).
- Rubidium Rb: from Latin rubidues (deep red) is not a red element; it is the typical metallic gray.
However, compound of rubidium, when burned in a flame, give out
a ruddy glow.
- Cesium Cs; renders a flame sky
blue, and is named from Latin for that color (caesius)
- Thallium Tl:
from Greek thallos (green shoot), because its compounds
turn a flame green-shoot green.
- Vanadium V: forms a series of compounds
that spans a rainbow of colors, and is named after the Scandinavian
goddess of beauty.
- Chromium Cr: from Greek chroma (color)
- Iridium Ir: from Greek and Latin iris (rainbow)
- Rhodium Rh: from Greek rhodon (rose)
- The nose is a constant companion of a chemical explorer.
- Bromine Br:
from Greek bromos (stench)
- Osmium Os: from Greek osme (smell)
- Many regions are named after locations that have a particularly
close association with their occurrence.
- Gallium (31 Ga): named by the discoverer
Francois Lecoq de Boisbaudran, supposedly for France (Latin: Gallia)
- Strontium Sr: name for Strontian,
in Scotland.
- Europium Eu: from Europe
- Americium Am: from America
- Scandium Sc: from Scandinavia
- Francium Fr: from France
- Germanium Ge: from Germany
- Rhenium Re: from Rhine (Latin: Rhenus)
- Ruthenium Ru: from Russia (Latin; Ruthenia)
- Californium Cm & Berkelium Bk:
from University of California at Berkeley.
- Hafnium Hf: from Copenhagen (Latin; Hafnia)
- Holmium Ho: from Stockholm (Latin: Holmia)
- Lutetium Lu: from Paris (Lutetia,
City of Light)
- Yttrium Y: from the little Swedish
town of Ytteby
- Dubnium (105 Db): for Dubna,
the site of a Soviet contribution
- Hassium (108 Hs): for Hassia,
old name of Darmstadt, where the inventing German laboratory exists.
|
5.元素名の由来:
- 王国の探検が科学になると、その地域(元素)の命名はある程度システム化されてきた。
- 古代の名前は、その起源が失われたり、あるいは歴史の闇の中でほとんど気づかなくなる。
- 硫黄 S:サンスクリット語のSulvereから
- 鉄 Fe、金
Au、銀 Ag:アングロサクソン語のiron,
gold, seolforから
- 銅 Cu:ラテン語のcuprum、銅を多く産するキプロスから
- ナトリウム Na、カリウム
K:Humphry Davyはそれぞれの原料名のsodaおよびpotashから
- カルシウム Ca:ラテン語のCalx (石灰)
から
- マグネシウム Mg:ギリシアのテッサリ地区のマグネシアで発見された白土magnes
carneusから
- 窒素 N:ギリシャ語のnitornとgenos (niter giver)、硝酸塩を産するチリ硝石から
- 酸素 O:ギリシャ語のoxys(酸性の)酸素は一般的に酸を生成すると信じられていた。この考えはその後否定されたが、元素の名称としては残った
(例:塩素の場合)
- 一部の元素は色を基準として名付けられてきた。
- 塩素 Cl:薄黄緑色のガス。ギリシャ語のchloros (黄緑色)から
- ヨウ素 I:紫色の固体、ギリシャ語のioeides (紫色) から
- ルビジウム Rb:ラテン語の rubidues (深い赤) が語源だが、実は赤色の元素ではなく、メタリックグレーである。しかしルビジウム化合物の炎中の色は赤色に輝く。
- セシウム Cs:この炎は空色であるので、ラテン語の空色(caesius)
から
- タリウム Tl:ギリシャ語のthallos (緑の新芽)から。その化合物の炎は緑の若芽色である。
- バナジウム V:この一連の化合物は虹をかけたような色を呈するので、北欧の美の女神の名から
- クロム Cr:ギリシャ語のchroma (色)から
- イリジウム Ir:ギリシャ語とラテン語の iris (虹) から
- ロジウム Rh:ギリシャ語のrhodon (バラ)から
- 嗅覚は化学探査にとっていつも連れ添う仲間である。
- 臭素 Br:ギリシャ語のbromos (悪臭)から
- オスミウム Os: ギリシャ語のosme (smell)
- 多くの地域は、発見に至る特別な事情を反映して名付けられている。
- ガリウム 31番Ga:発見者F. L. de Boisbaudranがフランス人だったからか
(ラテン語:Gallia)
- ストロンチウム Sr:スコットランドのStrontianから
- ユーロピウム Eu:Europeから
- アメリシウム Am:Americaから
- スカンジウム Sc:Scandinaviaから
- フランシウム Fr:Franceから
- ゲルマニウム Ge:Germanyから
- レニウム Re:Rhine (ラテン語:Rhenus)
から
- ルテニウム Ru:Russia (ラテン語:Ruthenia)から
- カルフォニウム Cmとバークリウム
Bk:
Calfornia大 Berkeley校から
- ハフニウム Hf:Copenhagen (ラテン語: Hafnia)
から
- ホルミウム Ho:Stockholm (ラテン語: Holmia)
から
- ルテチウム Lu:Paris (ラテン語: Lutetia)から
- イットリウム Y:スウェーデンの小さな町Ytteby から
- ドブニウム 105番Db:ソ連のDubnaから
- ハッシウム 108番Hs:発見したドイツ研究所のあるDarmstadtの古称Hassiaから
|
>Top Eternal memorial:
- There are the people who find their eternal memorial in the kingdom.
- Hahnium (72
Hf): for Otto Hahn
- Curium (96 Cm): for Marie Curie
- Einsteinium (99 Eu): for Albert Einstein
- Fermium (100 Fm): for Enrico Fermi
- Mendelevium (101 Md): for Dmitri Mendeleev
- Nobelium (102 No): Alfred Nobel for stimulation to discovery, maybe, rather than discovery itself
- Lawrencium (103 Lr): for E.O.Lawrence,
Berkeley scientist
- Rutherfordium (104 Rf): for Ernest Rutherford
- Seaborgium (106 Sg): for Glenn
Theodore Seaborg
- Bohrium (107 Bh): for Niels Bohr
- Meitnerium (109 Mt): for Lise Meitner,
Hahn's coworker
- Gods as well as mortals have lent their names.
- Titanium Ti: from Titans,
the children of Gaia, the Greek earth goddess.
- Promethium Pm: from Prometheus
- Mercury Hg: from fleet-footed Mercury
- Nickel Ni and Cobalt
Co : from German words for "goblin" (Nickel and Kobold)
- The most memorable characteristic, or named by mistake:
- Dysprosium Dy: it was very difficult
to isolate (Greek: dyprositos, "hard to get at")
- Oxygen O: already noted
- Molybdenum Mo: from Greek molybdos (lead)
- Platinum Pt: a diminutive of the
Spanish plata (silver)
- Celestial bodies have given their names to many elements.
- Selenium Se: from the moon (Greek: selene), for its silvery appearance.
- Cerium Ce: was discovered in 1803,
two years after the discovery of the asteroid Ceres.
- Palladium Pd: was discovered in
1803, at about the same time as the discovery of the asteroid Pallas.
- Plutonium PU & Neptunium
Np: elements made in war for purpose of war - bellicose
gods Pluto, Neptune.
|
この王国に永久に名前を刻んだ人々がいる。
- ハフニウム 72番Hf:Otto Hahnから
- キューリウム 96番Cm:Marie Curieから
- アインスタイニウム 99番Es:Albert Einsteinから
- フェルミウム 100番Fm:Enrico Fermi から
- メンデレビウム 101番Md:Dmitri Mendeleevから
- ノーベリウム 102番No:Alfred Nobelから、おそらく発見者としてよりも発見への奨励者として
- ローレンシウム 103番Lr:Berkeleyの科学者E.O.Lawrence から
- ラザフォーディウム 104番Rf:Ernest Rutherford から
- シーボルギウム 106番Sg:Glenn Theodore Seaborg から
- ボーリウム 107番Bh:Niels Bohr から
- マイトネリウム 109番Mt:Harnの共同発見者Lise Meitner から
- 神々もまた人間同様に名前を残している。
- チタン Ti:ギリシャの地の神Gaiaの子供Titansから
- プロメチウム Pm:プロメテウスPrometheusから
- 水銀 Hg:快速の商業・旅行の神Mercuryから
- ニッケル Niとコバルト Co;ドイツ語の小鬼Goblin (Nickel and Kobold)から
- 誤りによって名付けられた記念すべき名前:
- ジルプロジウム Dy:分離するのが非常に難しいというギリシャ語
(dyprositos)から
- 酸素 O:前述の通り
- モリブデン Mo:ギリシャ語のmolybdos (鉛)から
- 白金 Pt:スペイン語のPlata (銀)の愛称
- 展開も多くの元素の名前になっている。
- セレン Se:その銀色の類推でギリシャ語の月 (selene)
から
- セリウム Ce:小惑星Ceresの発見の2年後1803年に発見された。
- パラジウム Pd:1803年に小惑星Pallasの発見とほぼ同時期に発見された。
- プルトニウム Puとネプツニウム
Np:戦争目的で製造された。好戦的な冥界の神Pluto、および海洋の神 Neptuneから
|
>Top 6. Origin of the land:
- Big Bang:
The regions of the kingdom needed to form; they have not been there
forever. At the big bang (about 15 billion years ago), the cataclysm
that shook spacetime into being and marked the inception of our
universe. Hydrogen was the
very first element to be formed.
- In the violence of the first three
minutes;
hydrogen atoms smashed together, such was the tumult and density
of the primeval storm, and melded into helium.
- Two pillars fo hydrogen and helium:
Minutes passed, then yeas, thousands then millions of years,
and all there was of the kingdom remained the same. There was
as yet no hint of empire.
- The great clouds of the two primitive elements that pervaded
all there was of space were not completely uniform, and the
weak gravitational attraction between atoms slowly let to the
formation of regions of greater density and the slow denuding
of others. The universe became lumpy.
- Dense cloud:
Within the enormous cloud of greater density there were smaller
regions of even greater density. In due course, those smaller regions
were to become stars, and the great regions that contained them
were to become the galaxies.
- The formation of the stars opened up new opportunities, and
soon the surface of the imaginary ocean was broken by the gradual
appearance of new regions of the kingdom
- Origin of the elements:
The source of these new lands was the turmoil within the stars.
As stars formed, the hydrogen atoms within them were given new opportunities
to collide with one another. Hydrogen smashed against hydrogen and
added a little more helium to the kingdom. The energy released in
this process of nuclear fusion is the fuel that lights the stars.
Moreover, the process of fusion gave rise to other elements; hydrogen
fused with helium, and lithium sprang from the sea. lithium collided with hydrogen, and helium
with helium, and beryllium was born.
- Structure of atom:
The pebbles of the land are not solid, like real pebbles, but have
an inner structure. An atom is in fact seemingly almost nothing.
Only a superhumanly sharp eye will catch sight of a microscopic
dot at the center of the gossamer. This massive yet microscopic
dot is the nucleus of the atom. Nuclei are made up of two types
of fundamental particle, protons and neutrons.
- An atom consists of a cloud of electrons surrounding a minute
central nucleus; relatively, as about the size of a fly at the
center of a football stadium.
|
6.元素王国の起源:
- ビッグバン:
王国の地域は作られなければならなかった。その土地は永久に存在していたのではなかったのだ。約150億年前のビッグバンの爆発によって時空間が存在するようになり我々の宇宙の始まりが記録された。水素はまず最初の元素として形成された。
- 最初の3分間の猛威の中:
水素原子は激しくぶつかり、この原始の嵐の激動と濃縮によってヘリウムが融合された。
- 水素とヘリウムだけの二柱:
何分か、何年か、そして何十億年かが経過したが、王国のすべては同じ様子であった。帝国と呼べるようなものは何もなかった。
- 空間のすべてを満たしていた2つの元素の雲は完全に均一ではなかった。原子間に働く弱い重力による引力がやがてより密度の濃い領域となり、他の領域から元素をはぎ取っていった。宇宙に塊ができてきたのである。
- 濃縮した雲:
雲が高度に濃縮した中に、さらに高密度の狭い領域が形成された。そうしてこの狭い領域はやがて星々となり、それらを包む広い領域は銀河へとなっていった。
- 星々の形成は新たな機会を拡げてくれた。いわば海の表面から王国の新たな地域が徐々に姿を現し始めたのである。
- 元素の起源:
これら新たな土地の原料、即ち多くの元素の起源は、星々の中の水素原子が相互に衝突することで生まれた。水素同士が衝突することで王国には若干のヘリウムが追加された。このプロセスを通じて放出された核融合のエネルギーは星々を輝かせる燃料となった。さらに核融合プロセスは他の元素を生じさせた。水素がヘリウムと融合することでリチウムが生じた。リチウムは水素と衝突し、またヘリウム同士が衝突することでベリリウムが生まれた。
- 原子の構造:
この土地の石は、本当の石のような固体ではなく、内部構造をもっている。原子は実際にはほとんど何もないように見える。超人的な鋭い眼力でなければ、このクモの巣の中心にあるミクロな点を見つけることはできない。このミクロな点こそが原子の核である。核は基本的な2種類の基本粒子である陽子と中性子からなる。
- 原子はその中心の核を取り巻く電子のクモからなる。核の相対的なサイズは、サッカー場の中心にいる一匹のハエのサイズである。
|
>Top The interior of stars:
- The stability of nuclei in the hot tumult of the interior of stars
is a matter of the greatest importance. Collisions take place every
billionth of a second. Nuclei survive because their protons and
neutrons stick together as a result of a special force (strong force).
A nucleus can survive only if there are enough neutrons to provide
an additional source of the strong force without contribution to
the repulsion.
- Beryllium (4 protons
and 5 neutrons) and boron (5 protons and 5-6 neutrons) just manage to survive, but they are
far from abundant in the universe, for many were shaken apart almost
as soon as they were formed. Much of the lithium, beryllium, and
boron we now have are fragments, chipped from larger nuclei.
- Carbon:
There is something rather special about a nucleus of carbon which
enables it to form quite rapidly - its technical term is resonance.
Without that resonance, there would be no life. Carbon is the fourth* most abundant element in the universe. (*The originally described 'third.') Moreover, the formation
of carbon opens the door to the nucleosynthesis of other elements.
- Along the northern shore, carbon, oxygen, and neon are crests
and nitrogen and fluorine are troughs of the generally falling
terrain. If there are even numbers of protons and even numbers
of neutrons, then especially stable stacking patterns can form.
- Iron core:
After iron the nuclei become so large that the protons and the neutrons
are not able to interact with one another as strongly as is the
case in smaller nuclei. If a star were simply to burn to its death,
then the cinder left behind would be iron alone.
- 10^7 K: (107)
The first stage in the life of newly formed star begins when its
temperature has risen to about 10^7 K. This is the hydrogen-burning
stage of the stars's life cycle. At the same time, the outer regions
are pushed away from the central region.
- Now helium burning can begin in the dense hot core, and helium
nuclei fuse into beryllium, carbon, and oxygen.
This phase continues until the helium in the core is exhausted
and carbon and oxygen are present in approximately equal proportions.
- 10^9 K: (109)
At the end of the helium-burning phase, the inner regions of the
core again contract and the temperature rises once more to 10^9
K, and carbon and oxygen burning can begin. These processes result
in the formation of elements including sodium, magnesium, silicon,
and sulfur.
- When the stellar core has been depleted of carbon and oxygen
and is rich in silicon, the silicon-burning phase can begin,
and silicon is converted to sulfur, argon,
and other heavier elements. if contraction can raise the temperature
to about 3 billion degrees, then the equilibrium phase of the
star's life cycle begins, and elements close to iron are formed.
- At some stage of neutron accumulation, the nucleus becomes
so unstable that it spits out an electron - in effect, a neutron
has collapsed into a proton and a new, heavier
element has been formed.
- Star collapse:
As a star consumes atomic nuclei, there comes a stage at which its
center is old and worn, depleted of fuel. At that stage, the outer
regions of the star may collapse, like a falling roof. The falling
matter crashes onto the star's dense core and bounces back; in this
way, a star may shrug off its outer regions, scattering them through
space.
- Space no long contains only tenuous clouds of primordial hydrogen
and helium, for now there is an important contamination.
- Stars of different mass burn in different ways; some never
reach equilibrium; some never even reach the helium-burning
stage; some burn rapidly, others slowly.
- After their birth, the elements had a gentler history, freed
from the angry turmoil of stellar interiors.
- Solar system:
It is 4 or 5 billion years ago, ten billion years after the universe
began. The dirty cloud condenses, as dirty clouds do when gravity
can draw the particles together. Eventually it bursts into nuclear
activity, releasing energy as hydrogen fuses into helium. A crucial
remnant remains, encircling the incandescent star, bumping together
and sticking together as grains, then rocks, then boulders, then
planetesimals. One of these spheres becomes recognizable as the
molten planet: Earth.
- Fate of the kingdom:
We have seen a little of the distant past and of the recent past.
What, though, of its future? Is the kingdom eternal? A likely (but
not certain) scenario is that in at distant time, perhaps 10100
(googol) years into the future, all matter will have decayed into
radiation. Gradually the peaks and dales of the kingdom will slips
away and Mount Iron will rise higher. But even iron will decay,
and lone pinnacle will sink below the waves.
- More distant era:
All radiation will have been stretched out into flatness as the
universe expands, leaving no imprint. Now the universe will be no
more than dead, flat spacetime. All that once was, including the
memory and the knowledge of what one was, will have vanished.
|
星の内部:
- 星の内部の激しい熱の中でも原子核が安定していることは非常に重要なことである。衝突は10億分の1秒毎に発生するのである。原子核は、その陽子と中性子が特別な力
(強い核力) によって堅く結びついているが故に生き延びられる。原子核は十分な中性子があると反発力を増やすことなく強い核力が増すので生存できるのである。
- ベリリウム (陽子4個と中性子5個)
とホウ素 (陽子5個と中性子5-6個)はなんとか生存できるが、宇宙では数が多いとは言えない。その多くは生成されるや否や分裂してしまう。現在あるリチウム、ベリリウム、ホウ素はその多くは、大きな原子核から分裂した破片である。
:
- 炭素:
炭素の原子核については特別なことが起こることで急速に生成されることが可能となった。それは共鳴と呼ばれる。この共鳴がなければ、生命は誕生しなかった。炭素は宇宙で4番目に豊富な元素である。 (原文には3番目とある。) 更に、炭素の生成は他の元素の核合成の道を切り開いた。
- 王国の北側海岸に沿って、炭素、酸素、ネオンが山頂であり、窒素とフッ素は全般的に落ち込んでいる窪地となっている。偶数個の陽子と偶数個の中性子
(偶・偶核) があると特に安定的な詰め込みパターンが形成されるのである。
- 鉄のコア:
鉄以降の原子核は大きすぎるので、陽子と中性子は小さな原子核の場合のように強く相互作用することができない。星が単純に燃え尽きて死んでしまえば、残る灰は鉄だけとなろう。
- 1000万度K:
新たに生成された星の寿命の最初の段階では、その温度が1000万度程度に上昇する。これは星の寿命の中で水素燃焼段階である。同時に、外側の領域は中心部から押し出される。
- 濃縮した灼熱のコア部分ではヘリウムの燃焼が始まる。ヘリウムの核融合によって、ベリリウム、炭素、そして酸素が生成される。この段階はコアにおいてヘリウムが消費されて、炭素や酸素とほぼ同じ量になるまで継続する。
- 10億度K:
ヘリウム燃焼段階の終わりには、コアの内部は再び縮退し、温度がさらに10億度Kに上昇し、炭素や珊瑚が燃焼し始める。これらのプロセスによってナトリウム、マグネシウム、ケイ素、硫黄などの元素が生成される。
- 星のコアから炭素や酸素がなくなり、ケイ素が増えてくるとケイ素燃焼段階が始まり、硫黄、アルゴン、その他の重い元素が生成される。縮退によって温度は更に上昇して30億度になり、星の寿命の平衡段階が始まる。そして元素はすべて鉄になってしまう。
- 中性子の集積するある段階で、原子核は不安定となり、電子をはき出すようになる。この結果、中性子は陽子になって新たなより重たい元素が生成される。
- 星の崩壊:
星が原子核を消費し尽くすと、その中心部は燃料がなくなり、古く衰弱する段階となる。その段階で星の外側が、天井が崩れるように崩壊することになる。崩壊してくる物質は星の濃縮した中心部へ落ち込み、そこから跳ね返る。こうして星は外側の領域部分を空間にまき散らすことになる。
- 空間はもはや原始の水素とヘリウムだけの希薄な雲だけを含むものではなくなる。今や重要な元素の混じったものであるのだ。
- 星々は、それぞれ異なる重量に燃え方も異なる。ある星は平衡状態に達しないし、他の星はヘリウム燃焼段階に達しない。また急速に燃焼する星もあれば、ゆっくり燃焼する星もある。
- 元素は星の内部の激動の中から誕生した後では、比較的静かな時間を過ごしてきた。
- 太陽系:
この宇宙が始まってから100億年ほど経過した40-50億年前のことである。汚れた雲は、重力によってその粒子が引き寄せられるに従って濃縮していった。その結果として原子核反応が始まり、水素がヘリウムに融合されることでエネルギーが放出される。その残留物は白熱の星を集会し、
互いに衝突し、くっつき合って粒子となり、石となり、大きな岩石となり、そして小惑星となっていった。これらの天体の一つは説けた惑星へと成長していった。地球である。
- 王国の運命:
我々は遠い過去から近いの過去までを見てきた。しかし未来は一体どうなるのだろうか。この王国が永遠に続くのか。確実ではないが一つのあり得る遠い未来のシナリオはこうである。10^100年後の未来には、すべての物質は崩壊して放射線となってしまう。王国の山や谷は徐々に滑り落ち、鉄の山だけがより高くそびえるだろう。しかしやがては鉄も崩壊していき、孤独な尖塔も波間に沈んでしまう。
- さらに遠い将来:
すべての放射線は宇宙の膨張にともない、平坦に引き延ばされていく。そして宇宙には死だけの平坦な時空間が残される。過去に存在したすべてのもの、かつて存在した記憶も知識も含めて、すべてが消え去っていくだろう。
|
>Top 7. Abundance of atoms:
Abundance
in the crust |
O |
2900 |
Si |
1000 |
Al |
305 |
Ca |
103 |
Na |
103 |
Fe |
101 |
Mg |
96 |
K |
54 |
Ti |
12 |
P |
3.4 |
F |
3.3 |
Mn |
1.7 |
C |
1.7 |
- Abundance in the crust (left) and in the solar system (right): in
terms of the number of atom per 1000 Si atom.
Abundance in the solar system is derived from the analysis
of solar wind and stone meteorite called C1chondrite.
(Source: Dictionary
of Geology, Heibonsha1970, and Rikanennpyo, Science chonology, Maruzen
2001) |
7. 元素の存在度:
-
Abundance
in the cosmos |
H |
27900000 |
He |
2720000 |
O |
23800 |
C |
10100 |
Ne |
3440 |
N |
3130 |
Mg |
1074 |
Si |
1000 |
Fe |
900 |
S |
515 |
Ar |
101 |
Al |
85 |
Ca |
61 |
地殻における元素の存在度 (差表)および太陽系での元素の存在度。Siを1000とした元素組成。
- 太陽系の存在比は、太陽風および石質隕石 (C1コンドライト)の分析から得られる。
- (出典:地学事典、平凡社1970 および理科年表、丸善2001)
|
>Top 8. Cartographers:
- Johann Dobereiner, German chemist:
In 1829, He pointed out that the triad's central member was the
arithmetic mean of its two outer members: he identified iron, cobalt,
and nickel as triad. Elsewhere, he linked chlorine, bromine, and
iodine, and calcium, strontium, and barium. Few chemists in the
late 18C and early 19C believe that there was an arithmetic pattern
to matter. Matter was tangible; numbers were abstract.
- Beguyer de Chancourtois, French geologist:
In 1862, he arranged the elements on a spiral inscribed on a cylinder.
He noted a periodicity of properties, with similar elements recurring
after every seventh element.
- John Newlands, English chemist:
In 1864, he noticed that, as in a musical scale, harmonies among
the elements were seen in every eight steps. Thus, he proposed that
elements lay in octaves, and to a certain extent he was correct.
- He was laughed to scorn: "Why did not Mr. Newlands try
listing the elements alphabetically instead?"
- Julius Lothar Meyer, German chemist:
In 1864, he showed that the ability of elements to form compounds
with one another varied periodically with atomic weight, and put
forward an abbreviated chart of the kingdom. He found that by plotting
atomic volume against atomic weight a rhythm emerged Newlands' octaves
were certainly there.
- Dmitri Ivanovitch Mendeleev (1834-1907), Russian
chemist:
In 1869, he found that by arranging the elements in order of increasing
atomic weight, many of which were then known with reasonable accuracy,
and having the courage to leave gaps where the pattern seemed to
need them.
- Mendeleev knew only 61 elements, compared with 100 or so we
now know.
- According to an order based on atomic weight alone, he would
have had cobalt and nickel switch places, and the same with
tellurium and iodine. He ignored the masses of the atoms in
these cases, and used his nose to assign the elements to their
appropriate groups.
|
8. 地図の製作者:
- Johann Dobereiner、独の化学者:
1829年、三組の中心の元素は、両隣の元素の算術平均になっていることを指摘した。三組とは、鉄、コバルト、ニッケルであり、他の三組には、塩素、臭素、ヨウ素、そして、カルシウム、ストロンチウム、バリウムである。18世紀末および19世紀初めには、算術的なパターンが物質に作用していることを信ずる化学者はいなかった。物質は現実であるのに対し、数字は抽象なのである。
- Beguyer de Chancourtois、仏の地質学者:
1862年に。元素を円柱に巻き付けると、各々7番目の元素毎に元素の性質が周期的に現れることに注目した。
- John Newlands、英の化学者:
1864年に、元素の間には、音符のように各々8段階毎に調和が見られることに注目し、元素はオクターブに配置していることに注目した。これはある程度まで正しかった。
- 彼の説は嘲笑を受けた。「代わりに元素をアルファベット順に並べたら?」と。
- Julius Lothar Meyer、独の化学者:
1864年に、元素が化合物を生成する能力は元素重量に従って周期的に変化して現れることを示し、王国の簡略化した地図を作成した。彼は、原子重量に対し原子体積をプロットすることで、Nelandsのオクターブのリズムが確かに存在することを発見した。
- Dmitri Ivanovitch Mendeleev、露の化学者:
1869年に、彼は、それまで相当の精度で知られていた元素を重量の順番で並べ、またパターンにとって必要な部分は空白のまま残すことで、元素を配置してみた。
- 当時メンデレーエフは現在の100個余に対して61個の元素 しか知らなかった。
- 元素重量だけの順番でいくと、コバルトとニッケルの所とテルルとヨウ素の所の順番が逆転する。彼はこれらの場所の原子質量は無視して、直感を活かして元素を適切なグループへ配置した。
|
>Top 9. Law of the interior:
- Kingdom of the elements are far simpler than those that govern
our own lives. Quantum mechanics is necessary when we speak of atoms,
being microscopic. Energy can be transferred to an object only in
discrete amounts called quanta, not smoothly and continuously, as
was supposed in classical physics.
- An atom of an element is a gossamer entity, more space than substance.
It consists of a massive but minute central nucleus surrounded by
almost empty space, pervaded by the electron.
- John Dalton at the start of 19C, inferred from
his measurements that some unchangeable entity was involved in chemical
reactions.
- J.J. Thomson: showed, by using cathode-ray tube,
that a certain kind of fundamental particle (electron) could be
stripped out of any element.
- Michael Faraday: was confident that electricity
was bound up in some way with the composition of matter. After all,
electrolysis had shown that matter could be wrought into different
forms by the passage of an electric current.
- Ernest Rutherford: in 1910, shot alpha particles
formed by the radioactive decay of heavy elements at a thin sheet
of gold foil. While most of the particle sailed right through the
foil, some were scattered by it, and a few were reflected right
back to the source. He announced in 1911 that atom's positive charge
was concentrated into a massive central speck, and that most of
the rest of the atom was empty space. He concluded, there were not
thousands of electrons in an atom, but a few dozen at most.
- Henry Moseley: determined atomic number of an
element, then regarded as the number of units of positive charge
on its nuclei.
- We can now see why atomic weight broadly correlates with the periodicity
of the kingdom, and also why it sometimes fails.
- Determination of atomic weight is not the mass of a single
atom. Instead, we measure the average mass of a sample,
which normally contains several different isotopes.
|
9.内部の法則:
- 元素の王国は、我々の生活を支配するよりも遙かに単純である。ミクロの世界の原子を相手にするには、量子力学が必須となる。ある対象に対するエネルギーの伝達は、量子と呼ばれる離散的な量によってのみ行われ、これは古典物理学のようにスムーズでも連続的でもない。
- 元素の原子はクモの巣のような状態で、物質より空間だらけである。それは重たくで極小の中心核が、電子が広がったほとんど空の空間によって囲まれている。
- John Daltonは、19世紀初めに、化学反応の実験をとおして、変化しないいくつかの実体があることを推論した。
- J.J. Thomsonは、陰極線管を遣ってある種の基本的な粒子 (電子) がどの元素からも取り出せることを示した。
- Michael Faradayは、物質の構成においてはどうやら電気が結びついていることを確信した。そいてついに電気分解によって電流を流すことで、物質は別の形態に分解され得ることを示した。
- Ernest Rutherfordは、1910年に重たい元素の放射性崩壊によって作られたアルファ粒子が金の薄膜に照射した。その粒子のほとんどは金箔を通過したが、一部は金箔によって散乱し、小数は元へ反射された。彼は1911年に原子の正電荷は重たい中央の核に集中しており、原子の残りのほとんどは空間しかないことを発表した。彼は、原子の電子は数千もあるのではなく、せいぜい数十程度であると結論づけた。
- Henry Moseley:は、元素の原子番号を決定した。それは当時は核の正電荷の単位数であるとみなされていた。
- 今や、我々は、原子質量が広い意味で王国には周期性に関連しており、また時にはそれが成立しない理由を理解できる。
- 原子質量の決定は一つの原子の質量だけではきまらない。我々は採取した原子に含まれるいくつかの異なる同位体の平均質量を測定している。
|
>Top 10. Laws of the exterior:
- Hantaro Nagoka: Japanese physicist pictured in
1904 that atom is of tiny planet-like electrons orbiting a central
sunlike nucleus.
- Erwin Shrodinger, Austrian physicist in 1926
pictured a hydrogen atom: the electron is distributed as a spherical
cloud around the nucleus. This cloudlike distribution of an electron
is called an atomic orbital. An electron cannot be found
at a particular point; all we can do is state the probalitily that
it will be found there.
- Hydrogen model:
A spherical orbital of hydrogen is called an s-orbital.
If enough energy is pumped into a hydrogen atom, the electron can
be puffed up into a second sort of s-orbital. the first orbital
is called a 1s-orbital ,
then the sencond is 2s-orbital, the third
is 3s-orbital.
- When the electron is given enough energy to occupy a 2s-orbital,
it can also form a cloud of an entirely diffeerent shape - a two-lobed p-orbital.
- The orbitals available to an electron in a hydrogen atom are called s, p, d,
and f, according to the number of lobes
they have. (s means sharp, p=principal, d=diffuse, and f=fundamental)
- There is only one orbital available to an electron
in the ground state, and four available in the first higher-energy
state. There are two elements in Period -1 (H and He), and eight
elements in Period-2 (from Li to Ne), which is twice the number
of orbitals'.
- There are typically ten elements in the Isthmus for each period
of the kingdom, which is exactly twice the number of d-orbitals.
The Southern Island (f-block), where there
are 15 elements in each row, rather than 14 by twice of seven f-orbitals.
The total number of regions across the kingdom in Period-6 is 32.
that number is twice the sum 1+3+5+7=16 for the total number of
orbitals.
- First, the occupation of orbitals is governed by Pauli's exclusion
principle - that no more than 2 electrons can occupy any given orbital.
Second, the conspiracy of shielding and penetration ensure that
the 2s-orbital is somewhat lower in energy
than the p-orbitals of the same rank.
by extension, ns- and np-orbitals
in turn have a lower energy than nf-orbitals.
- One concerns the numbering of the groups - the chart's vertical
columns - from I to VⅢ. We can now see that these numbers are
exactly the total number of electrons in the outermost rank of orbitals.
Thus, lithium (Group-I) has one electron, beryllium (Group-Ⅱ) has
two, boron (Group-Ⅲ) has a total thee (two s and one p), and so on, where neon (Group-ⅤⅢ)
has eight.
- The groups of orbitals of the same type within a shell are said
to constitue a subsehll of that shell. Thus, the 2s-orbital
constitutes one subsehll of the second shell of an atom, and so
on. When a subshell has its full complement of electrons (2 for
an s-subshell, 6 for a p-subshell,
10 for a d-subshell, and 14 for an f-subshell),
we say that the subshell is complete. The d-
and f-subshells do not need to be complete.
The outer shell is called the valence shell.
|
10. 外部の法則:
- 長岡半太郎: 日本の物理学者。1904年に原子は小さな惑星状の電子が、中心にある太陽のような核を周回しているとして描いた。
- Erwin Shrodinger, オーストリアの物理学者。1926年に水素原子を描写し、電子は核の周りに球形の雲のように分散しているとした。この雲のような電子の分布は電子軌道と呼ばれる。電子は特定の点に見いだすことは不可能である。我々にできることはそこに見いだす確率を述べることである。
- 水素モデル:
水素の球形の軌道はs 軌道と呼ぶ。もし水素原子に十分なエネルギーを注入すると、電子は2番目のs 軌道に移る。最初の軌道は1s-orbital 、2番目の軌道は2s-orbital、3番目の軌道は3s-orbitalと呼ぶ。
- 電子に十分なエネルギーを与えると2s-orbitalに占めるようになる。それは2葉(ローブ)をもつ全く異なる形の雲( p-orbital)を形成する。
- 水素原子での電子の軌道は葉(ローブ)の数によって s, p, d, fの各軌道を取る。
(s=sharp, p=principal, d=diffuse, f=fundamentalの意)
- 基底状態の電子は唯一の軌道しか取れない。それより高いエネルギーでは4つ軌道の状態を取れる。第一周期 (HとHe)では2つの元素が、第二周期
(LiからNe) では8つの元素があり、その数は軌道数の2倍である。
- 王国の地峡には、10個の元素があり、それはd軌道の2倍の数である。南島
(f ブロック)には、各行にはf 軌道の2倍の14ではなく15の元素がある。第6周期の王国を横断する元素の数は、32個であり、その数字はすべての軌道の数、1+3+5+7=16の2倍である。
- まず、軌道の占有はパウリの排他原理に従う。即ち、各軌道には2つ以上の電子は存在できない。次に、遮蔽と貫通の関係によって、2s 軌道は同じランクのp 軌道よりエネルギー準位が低い。同様にns 軌道やnp 軌道はnf 軌道に比べてエネルギー隼位が低い。
- 周期律表の縦の列の I属からVIII属についての各グループの数については、最外殻の軌道にある電子の数と一致する。リチウム (
I属) の電子は1個、ベリリウム ( II属)は2個、ホウ素 (III属)は3個で、これはs 軌道2個、p 軌道1個の合計に相当する。以下同様で、ネオン (VIII属)は8個である。
- ある殻の中にある同じ型の軌道グループには、その殻の中にサブ殻がある。それは2s 軌道と表し、原子の2番目にある殻のサブ殻を示す。各サブ殻には電子が完全に入る場合の数が決まっている。即ち、s 殻には2個、p 殻に6個、d 殻に10個、f 殻に14個入ると、サブ殻が満杯であることを意味する。但し、d 殻とf 殻は必ずしも満杯にならない場合もある。最外殻は原子価殻と呼ばれる。
|
>Top 11. Regional administration:
- masses of the atoms:
vary almost systematically
throughout the kingdom. The occasional fault is accounted for because
atomic weight is calculated as an average mass of a sample.
- atomic diameter:
fell from west to east across a period and increased from north
to south: successive periods of the kingdom correspond to the formation
of a new electron shell for the atom. The shrinkage
from west to east across a period is not quite as simple to explain,
for at first it seems peculiar that atoms shrink as the number of
electrons increases. As we travel east across a period, this increasing
nuclear charge attracts the surrounding electrons more strongly.
- Balanced forces:
We see that the sloping landscape of atomic diameter is the outcome
of a competition of finely balanced forces. The
effect of nuclear attraction only just dominated the landscape;
were it a little weaker, the kingdom would tilt the other way. The
kingdom is like a parliamentary democracy with almost equal party
representation; sometimes the left will win, sometimes the right.
- Peculiar leveling of the plain in the landscape of diameters in
the South (f-block):
The nuclear charge is steadily increasing as we step from west to
east along this secondary isthmus, as so we can expect the atoms
to contract. The f-electrons are distributed
like clouds of a very spindly shape, and they do not effectively
shield the electrons from the increasing charge of the nucleus.
Thus we can expect the effect of nuclear attraction to be dominance,
and for these to be a substantial contraction of the atoms across
the f-block.
- The landscape of ionization energy:
Broadly speaking, it is low in the Western Desert and high in the
nonmental regions of the Eastern Rectangle. This landscape slopes in the opposite direction , in general, from the landscape
of diameter. As we travel from southwest to northeast, atoms become
smaller, and the outmost electron is closer to its nucleus. The
grip of the nucleus on the electron is tighter, and so the ionization
energy rises. In the Western Desert, ionization energies are small
enough for these atoms to lose their electrons readily (prevailing
sea of electrons).
- d-block:
Here is the d-block with electronic structure like [Ar]4s^2 3d^5 (that
of Mn), the energy of chemical reactions is sufficient to remove
the two s-electrons and a variable number
of d-electrons. As a result, all manner
of different types of cation can be formed. A major beneficiary
of these relaxed circumstances are the processes of life.
- For example, iron appears as four bloody eyes in the center of the hemoglobin molecule, and its readiness to switch its complement of electrons
enables it to accommodate an oxygen molecule.
- In the photosynthetic process, it is manganese that deploys the electrons that the sun's energy releases.
- The chemical industry draws intensely from the Isthmus, because
almost all its products are manufactured using catalysts.
- Nitrogen is fixed through the agency of iron.
- Bacteria discovered how to make use of molybdenum to fix nitrogen.
- Sulfuric acid is made with platinum and vanadium as
catalysts,
- Nitric acid is made with rhodium as a catalyst.
- Hydrocarbons pumped from carbon's lairs beneath the Earth.
- The sizes of anions:
An anion is larger than its parent atom because the additional electron
puffs the atom up against the pull of the central nucleus.
|
11. 地域の政治:
- 原子質量:
王国全体を通じて原子質量の変化は規則的である。所々の例外の水は原子質量が試料の平均重量で計算されていることによる。
- 原子半径:
これは周期の西から東に向かって減少し、また北から南へ向かって増加している。それは王国の周期の連続は原子に新たな電子殻が作られることに対応している。周期の西から東へ向かって縮小している理由は簡単ではない。電子が増加するに従って原子が縮小していくように見えるのは奇妙に見える。ある周期で東へ移動すると原子核の電荷が増えることで周囲の電子をより強く引きつける。
- 勢力均衡:
原子半径のなだらかな傾斜は微妙な力のバランスの競合の結果である。原子核による引力の効果は地形を支配する。もしそれが少しでも弱ければ王国の傾斜は異なったはずである。この王国は勢力の拮抗する政党による議会制民主主義のようである。時には左派が、また別の時には右派が勝利したりする。
- 南部 (f ブロック) の原子半径地形の平坦な理由:
二番目の地峡に沿って西から東へ進むにつれば原子核の電荷は確実に増加していき、原子は収縮すると期待されるが、f 殻の電子はひょろ長い雲のような形で分布しているので、原子核の電荷の増加に対して電子を効果的に防御できていない。従って原子核の引力が強くなり、f ブロックを通じて原子は実質的に収縮している。
- イオン化エネルギーの地形:
全体として、西部砂漠地帯では低く、東部の非金属地帯では高い。この地形は原子半径の地形の傾きに比べると概ね逆方向になっている。我々が南西から北東へ移動すると、原子は小さくなり、最外殻の電子は小さくなり、そしてイオン化エネルギーは上昇する。西部砂漠地帯ではイオン化エネルギーは小さいので、この地帯の原子は電子を失いやすい
(電子の海となる)
- d ブロック:
d ブロックの電子構造は [Ar]4s^2 3d^5 (マンガンの場合)
のようになっており、化学反応のエネルギーによって2つのs 殻の電子は容易に移動してd 殻の電子数を変えてしまう。その結果、多くのタイプの陽イオンが作られる。このような寛大な環境が特に生命作用にとって好都合となっている。
- 例えば、鉄はヘモグロビン分子の中の4つの血液の目として登場し、鉄の電子の補完が用意であることで、酸素分子を運搬することが可能となる。
- 光合成においては、マンガンがうまく電子を配置して太陽のエネルギーを解放している。
- 化学工業は、この陸峡の元素から特に恩恵を得ている。ほとんどすべての生成物は触媒を利用して生産されている。
- 窒素は鉄の作用を通じて固定される。
- バクテリアは窒素の固定にモリブデンを活用することを発見した。
- 硫酸は白金とバナジウムを触媒として作られる。
- 硝酸はロジウムを触媒として作られる。
- 炭化水素の植物は地中に隠れた炭素を汲み上げて成長する。
- 陰イオンのサイズ:
陰イオンは、その元となる原子よりも大きい。追加の電子が中央の原子核の引力に対抗して、原子をふくらませるからである。
|
>Top 12. Liaisons and alliances:
- From a hundred or so elements, millions of such
alliances can be constructed, just as an infinite literature can
be forged from the letters of an alphabet.
- Compounds are intimate intermarriages of the atoms, not mere
mixtures. Such is the case with the liaisons that form the Earth's
core and its rock landscapes. Other liassisons are less stable.
Such is the case with many of the naturally organic compounds
based on carbon.
- Chemical bonds:
Valence (from Latin valete, strengh) is a term signifying
the power of atoms to form chemical bonds.
- Ironic bond:
is an interaction between the ions that atoms form, stemming
from the attraction between the opposite charges of cations
and anions.
- Covalent bond:
is a discreete combination of atoms, effected by the sharing
of electron pairs.
- Removal of one electron from each sodium atom, which requires
5.1 eV. Nevertheless, 3.6 eV of energy is released when an electron
enters a chlorine atom and forms a chloride ion.
- ionic solid - strucutre of sodium chloride:
There are six cations around each anion and six anions around each
cation.
- They are tough aggregates of ions stacked tightly toghether,
they are rigid, brittle solids. So ionic solids usually have
high melting points. When they dissolve in water, the ions drift
apart and become mobile conductios of electricity (electorolytes)
- Covalent bond:
When two atoms come together, the distribution of the electrons
of their valence shells is no longer confined to each atom alone
but now spread over both of the like a net. (molecular orbitals)
Only two electrons can be accommodated in one of these orbitals
(due to Pauli exclusion principle) In case of the covalent bonds
we do not have to worry about the huge investment, for electron
sharing invoves much less drastic redistributons of electrons.
- Molecular compounds are the soft face of
nature, and ionic compounds are the hard. The soft face of the
Earth - its rivers, its air, its grass, its forests, all of
which are molecular - and the harsh substuctures of the landscape,
which are largely ionic (like rocks and minerals).
- The overarching power of carbon:
The essential reason is carbon's intrinsic mediocrity, its lack
of self-assertion. It is neither an agressive shedder of electrons,
nor is it an avid receiver. Carbon is mild in its demand on the
alliance it makes. Moreover, it is even content with its own company,
forming chains, rings, and trees of atoms. By being in the middle,
undemanding and not particularly generous, it can spin lasting alliances
rather than hasty consiracies.
|
12. 連結と連合:
- 百幾つかの元素から、何百万という連合が作られる。それはあたかもアルファベットの文字から無限の文学が生まれるようなものである。
- 化合物は原子の緊密な近親結婚であって、単なる混合ではない。地殻を構成し、その岩石が地形を作るような安定的な連結がそうである。またもっと不安定な連結もある。炭素を基礎とした自然界の有機化合物の多くがそうである。
- 化学結合:
原子価 (ラテン語のvalete、力の意) とは、化学結合を作る際の原子の力を表す。
- イオン結合:
陽イオンと陰イオンが引き合うことで原子間のイオンの相互作用である。
- 共有結合:
電子対を共有することで生じる元素の離散的な連合である。
- ナトリウム原子から1つの電子を取り出すのに5.1 eVが必要であるが、1つの電子が塩素原子に入り込み塩素イオンを形成するためには3.6
eVのエネルギーが放出される。
- イオン性固体:塩化ナトリウムの構造
各陰イオンの周囲には6個の陽イオンがあり、各陽イオンの周囲には6個の陰イオンがある。
- それらはイオンが密集して詰まった強固な集合体であり、堅く、砕けやすい固体である。イオン性固体は通常融点が高い。水中に溶かすと、イオンが分離して電気を運ぶ移動体となる
(電解質)
- 共有結合:
2つの原子が一緒になると、それらの原子価殻の電子が各々の原子に閉じこめられずに、ネットの状態のように2つの周りに拡散する (分子軌道)
。2つの電子だけがこれらの軌道に収まる (パウリの排他原理による) 。共有結合の場合、大きな投資を気にしなくてよい。というのは電子の共有は電子の再配置のような劇的な状態ほどではないからである。
- 分子化合物は自然におけるソフトの面であり、イオン化合物はハードの面である。地球のソフト面は、川や空気や草や森などで、これらはすべて分子からなっている。一方地形の厳しい構造の多くのイオン化合物である。
(岩石や鉱物の如く)
- 炭素の包括力:
その主なな理由は、炭素が本質的に平凡であることである。それは自己主張が少ない。炭素は積極的に電子を放出もしないし、熱心に受け取りもしない。炭素は連合を形成する場合の要求も厳しくない。さらに炭素自身の内輪の会社に満足して、鎖や輪や系列を作っている。中央に位置していて、要求することは少ないが、特に寛容という訳ではない。それは継続的な連合を作り、急いだ共謀には乗らない。
|

 Atom's mass:
Atom's mass: c masses. The diameters are based on the lengths of the
bonds the elements form. Broadly speaking, the landscape of diameters
rises from north to south and falls from west to east, but there
are many exceptions.
c masses. The diameters are based on the lengths of the
bonds the elements form. Broadly speaking, the landscape of diameters
rises from north to south and falls from west to east, but there
are many exceptions.
 The broad trend is the ionization energy
generally increase from west to east across the kingdom and
decrease from north to south. The ionization energy of hydrogen
is 13.6 eV. The three highest peaks in the distance are helium
(24.6), neon (21.6), and fluorine (17.4). The low terrain
of the Western Desert should not come as a surprise; they
conduct an electric current, that is, the atoms that lie packed
together in the solid release electrons to a common pool that
lies like an ocean among the resulting cations.
The broad trend is the ionization energy
generally increase from west to east across the kingdom and
decrease from north to south. The ionization energy of hydrogen
is 13.6 eV. The three highest peaks in the distance are helium
(24.6), neon (21.6), and fluorine (17.4). The low terrain
of the Western Desert should not come as a surprise; they
conduct an electric current, that is, the atoms that lie packed
together in the solid release electrons to a common pool that
lies like an ocean among the resulting cations.
